par F5FOD, Jean-Pierre Waymel
AvertissementLe contenu de cette causerie n'est pas au programme de l'examen. Cependant nous avons estimé que vous pourriez être intéressés par le sujet traité. En effet, la plupart des diodes à semi-conducteur et une grande famille de transistors contiennent une ou des jonctions P-N. Le propos sera néanmoins fortement simplifié : pas d'appel aux mathématiques de la mécanique quantique ! 1. Un exemple d'association d'atomes : la molécule de chlorure de sodium, NaCl
Reprenons la structure de l'atome de Bohr pour le sodium (symbole : Na). Pour cet élément, le nombre atomique est égal à onze (le nombre atomique est le nombre de protons dans le noyau). Quand cet atome est neutre, il possède autant d'électrons, donc onze. Ces électrons se répartissent par couches successives autour du noyau, ici sur les couches K, L et M :
- couche K : 2 électrons,
- couche L : 8 électrons,
- couche M : 1 électron. Un atome de chlore (symbole : Cl) a un nombre atomique égal à dix-sept. Par conséquent, quand cet atome est neutre, il possède dix-sept électrons :
- couche K : 2 électrons,
- couche L : 8 électrons,
- couche M : 7 électrons. Dans cette causerie, ce sont les électrons des couches externes qui nous intéressent :
- ce sont eux qui sont les plus éloignés du noyau, donc moins soumis à son attraction,
- ce sont eux qui possèdent la plus grande énergie. Par ailleurs, un atome est « satisfait » s'il possède huit électrons sur sa couche externe (deux si cette couche externe est la couche K). C'est la règle dite « règle de l'octet ».
Supposons qu'un atome de sodium Na perde le seul électron de sa couche externe M :
- il devient positif car il était neutre au départ puis il a perdu la charge électrique négative d'un électron,
- on l'appellera « Na+ »,
- sa couche externe est maintenant la couche L contenant huit électrons ; l'atome est « satisfait » mais il n'est plus neutre. Il prend d'ailleurs le nom d'« ion ». Supposons aussi qu'un atome de chlore Cl reçoit un électron supplémentaire qui vient se loger sur sa couche externe M :
- il devient négatif car il était neutre au départ puis il a gagné la charge électrique négative d'un électron,
- on l'appellera « Cl− »,
- sa couche externe est toujours la couche M mais contenant maintenant huit électrons. L'atome est « satisfait » mais il n'est plus neutre. C'est aussi un ion. C'est exactement ce qu'il se passe dans une molécule de chlorure de sodium NaCl : l'atome de sodium « prête » un électron à l'atome de chlore. La molécule est électriquement neutre car elle contient finalement autant d'électrons (11 − 1 + 17 + 1 = 28) que de protons (11 + 17 = 28). Comme « + » et « − » s'attirent, les ions sodium Na+ et chlore Cl− s'attirent et la molécule NaCl reste stable, du moins si aucun agent extérieur ne vient la perturber… On dit que le sodium a une valence égale à I (« 1 » en chiffre romain) ou qu'il est monovalent car il prête facilement un électron dit « de valence ».
« Valence » : du latin « valere », être fort ! La couche externe est aussi appelée « couche de valence ».
De même, ici, on dit que le chlore a une valence égale à I car il reçoit facilement un électron « invité ». 2. Un autre exemple d'association d'atomes : le cristal de germanium ou de silicium
Un atome de germanium (symbole : Ge) a un nombre atomique égal à trente-deux. Quand cet atome est neutre, il possède donc trente-deux électrons :
- couche K : 2 électrons,
- couche L : 8 électrons,
- couche M : 18 électrons,
- couche N : 4 électrons. Un atome de silicium (symbole : Si) a un nombre atomique égal à quatorze. Quand cet atome est neutre, il possède donc quatorze électrons :
- couche K : 2 électrons,
- couche L : 8 électrons,
- couche M : 4 électrons. Les atomes de germanium et de silicium possèdent donc le même nombre d'électrons sur leur couche externe : quatre. Voici la structure de leur réseau cristallin :
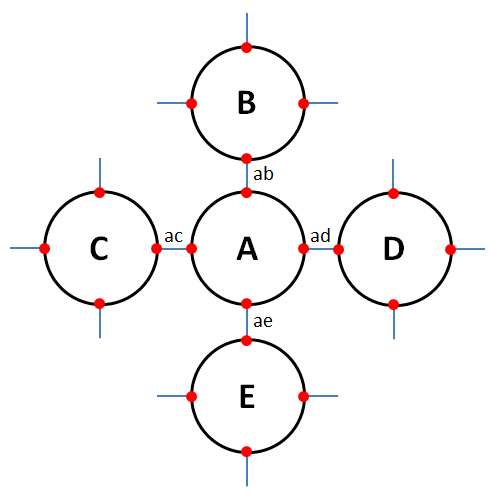
On pourrait croire qu'un cristal de germanium ou de silicium est un très bon isolant car il ne semble exister aucun électron libre susceptible de se déplacer. Que nenni, ce serait bien vite oublier les perturbateurs extérieurs ! Au premier chef de ces perturbateurs, citons l'agitation thermique. Puis les rayons alpha, les rayons gamma, les rayons X et plus généralement les photons qui bombarderaient le cristal. Le supplément d'énergie apporté par ces perturbateurs à certains électrons des couches externes des atomes va leur permettre de s'en échapper : c'est l'événement noté « 1 » :
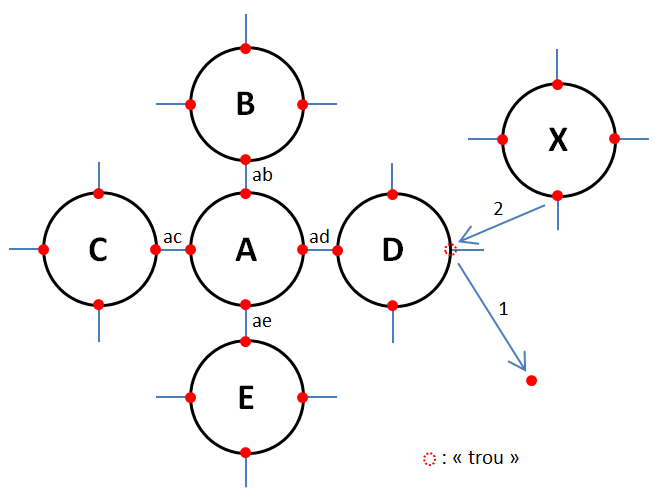
- la liaison covalente correspondante est rompue,
- il y a création d'« une absence » d'électron, absence que l'on nomme « trou »,
- l'ensemble de l'électron libéré et de ce trou constitue « une paire électron-trou ». L'atome D ayant perdu une charge électrique négatique devient alors chargé positivement :
- il attire un électron de la couche externe d'un atome proche, par exemple l'atome X,
- cet électron va quitter son atome X et aller se loger dans le trou précédemment créé dans la couche externe de l'atome D,
- c'est l'événement en cours noté « 2 » sur le schéma précédent, l'électron n'est pas encore parti de son atome X mais il s'y prépare ! L'électron parti de l'atome X a rejoint l'atome D. Ce faisant :
- pour l'atome D, la règle de l'octet est à nouveau satisfaite,
- il redevient électriquement neutre. L'atome X ayant perdu un électron de sa couche externe :
- un trou s'y crée,
- à son tour, l'atome X devient chargé positivement. Et le processus se répète ainsi d'atome en atome, au sein du cristal, dans les trois dimensions de l'espace. Nombre d'atomes et de paires électron-trou dans un cristal de silicium intrinsèque
Un cristal de semi-conducteur pur et sans défauts de structure est appelé "semi-conducteur intrinsèque".
Dans un centimètre cube de silicium intrinsèque et à 300 K, il y a :
N = 5 × 1022 atomes de silicium,
ni = 1 × 1010 électrons éjectés des couches externes,
pi = ni = 1 × 1010 trous créés dans les couches externes.
L'indice "i" rappelle ici le qualificatif "intrinsèque". Connectons maintenant une tension continue aux « bornes » du cristal, une pile par exemple :
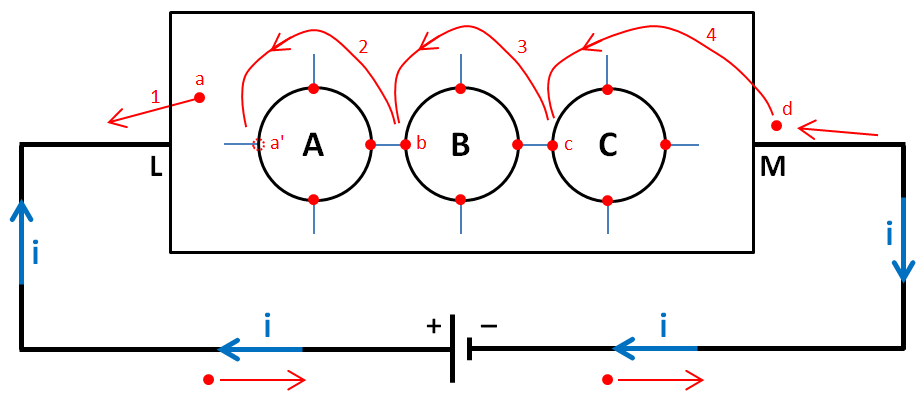
« 1 » : le pôle « + » de la pile attire l'électron « a » qui quitte le cristal. Il rejoint le pôle « + » de la pile comme nous l'avions étudié ici.
« 2 » : un électron « b » de la couche externe de l'atome B vient combler le trou « a' » de l'atome A afin que la règle de l'octet soit satisfaite pour cet atome A. Le départ de l'électron « b » crée un trou dans la couche externe de l'atome B.
« 3 » : un électron « c » de la couche externe de l'atome C vient combler le trou dû au départ de l'électron « b » afin que la règle de l'octet soit satisfaite pour l'atome B. Le départ de l'électron « c » crée un trou dans la couche externe de l'atome C.
« 4 » : le pôle « − » de la pile fournit un électron pour combler le trou dû au départ de l'électron « c » afin que la règle de l'octet soit satisfaite pour cet atome C. La pile a donc récupéré un électron sur son pôle « + » et a fourni un électron depuis son pôle « − ».
Bien entendu, ce processus imagé concerne simultanément de nombreux électrons arrachés par l'agitation thermique au sein du cristal. Un courant d'électrons circule donc de L vers le pôle « + » de la pile et de son pôle « − » vers M. Dans le cristal, il circule de M vers L. Le sens conventionnel du courant étant le sens inverse de celui des électrons, un courant conventionnel i circule, à l'extérieur de la pile, de son pôle « + » vers son pôle « − », ce qui est tout à fait classique ! On peut aussi remarquer que les trous se déplacent en sens inverse de celui des électrons !
Autrement dit, les trous se déplacent dans le sens conventionnel du courant, à l'inverse de celui des électrons : c'est logique puisque l'on peut considérer un trou comme une pseudo-charge positive… In fine, les mouvements des électrons dans un semi-conducteur et dans un métal conducteur tous deux soumis à une tension sont assez similaires. Cependant, à température identique, la densité d'électrons libres dans un semi-conducteur est beaucoup plus faible que la densité d'électrons libres dans un métal conducteur. D'où une conductivité beaucoup plus faible également et la justification du terme « semi-conducteur ». Rappelons que la conductivité (en siemens par mètre, S/m) est l'inverse de la résistivité (en ohm.mètre, Ω.m). Valeurs de résistivité ρ, en Ω.m, à 300 K
| Matériau | Résistivité | Type |
| Argent | 1,6.10−8 | conducteur |
| Cuivre | 1,8.10−8 | conducteur |
| Aluminium | 2,8.10−8 | conducteur |
| Germanium | 0,5 | semi-conducteur |
| Silicium | 2400 | semi-conducteur |
| Quartz | 1.1016 à 1.1018 | isolant |
| Verre | 1.1017 | isolant |
| Polystyrène | 1.1020 | isolant |
Les semi-conducteurs intrinsèques n'ont guère d'applications pratiques en électronique. Il va en être tout autrement si nous les « dopons » astucieusement avec certaines « impuretés ».
Considérons les atomes de phosphore (P), d'arsenic (As), d'antimoine (Sb) ou de bismuth (Bi). Ces atomes possèdent tous cinq électrons sur leur couche externe, soit un électron supplémentaire par rapport au silicium ou au germanium.
Prenons l'exemple concret d'un cristal de silicium pur dopé avec des atomes d'arsenic. Ces atomes d'arsenic vont venir s'intercaler dans le cristal de la façon suivante :
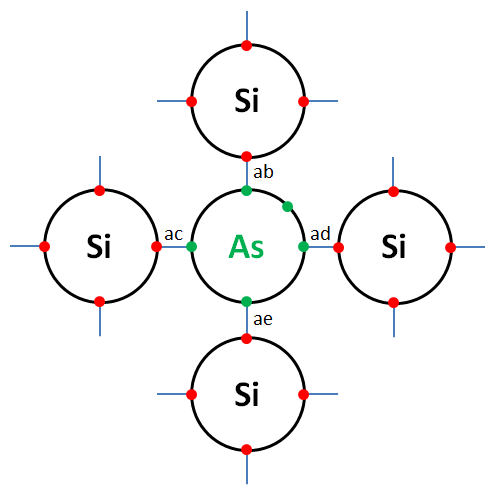
Quand ce cinquième électron est éjecté de son atome d'arsenic, la situation se présente ainsi :
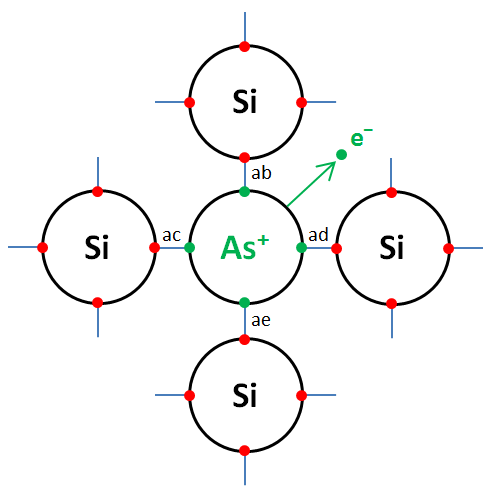
- Un électron est donc disponible : c'est un « porteur de charge négative ».
- N'oublions pas « l'activité intrinsèque » du silicium : l'apparition de paires électron-trou, toujours présente ! Les électrons de ces paires sont aussi des porteurs de charge négative tandis que les trous sont des « porteurs de charge positive ». Calcul des densités de porteur
Reprenons notre centimètre cube de silicium mais cette fois-ci dopé avec de l'arsenic.
Dans ce volume, à 0 K, il y a :
N = 5 × 1022 atomes de silicium,
ND = 1 × 1016 atomes d'arsenic (exemple concret). À 300 K, l'agitation thermique :
- crée les paires électron-trou à partir de certains atomes de silicium,
- éjecte un électron par atome d'arsenic. À cette température en effet, l'ensemble des ND atomes d'arsenic sont transformés en ions positifs. Appelons « p » le nombre de trous, porteurs de charge positive.
Appelons « n » le nombre total d'électrons éjectés, porteurs de charge négative : ceux provenant du silicium (les électrons des paires électron-trou) plus ceux provenant de l'arsenic.
Ces trous et ces électrons sont mobiles au sein du réseau cristallin, contrairement aux ions d'arsenic.
Comme le cristal de silicium dopé à l'arsenic reste électriquement neutre, nous pouvons écrire que le nombre total de charges négatives est égal au total de charges positives :
(1) ![]()
Lorsque l'équilibre thermodynamique est atteint (équilibres thermique, mécanique et chimique), cette loi nous dit que le produit des densités d'électrons et de trous (donc aussi le produit des nombres d'électrons et de trous par centimètre cube) est une constante, que le silicium soit dopé ou non.
Dans le silicium intrinsèque (sans arsenic), ce produit est égal à ni × pi avec ni = pi.
Dans notre silicium dopé avec de l'arsenic, ce produit est égal à n × p.
Appliquons la loi d'action de masse :
![]()
![]()
![]()
![]()
![]()
Maintenant, calculons p :
![]()
Dans notre centimètre cube, les n porteurs de charge négative sont donc beaucoup plus nombreux que les p porteurs de charge positive : ici 1012 fois plus nombreux !
C'est pourquoi les porteurs de charge négative sont appelés « porteurs majoritaires » tandis que les porteurs de charge positive sont appelés « porteurs minoritaires ».
Tout à fait logiquement, le cristal de silicium dopé avec de l'arsenic est appelé « semi-conducteur extrinsèque de type N » car les porteurs majoritaires sont des électrons donc des charges négatives.
Les atomes initiaux d'arsenic sont appelés « donneurs » car ils donnent leur cinquième électron externe en se transformant en ions chargés positivement.
Moyen mnémotechnique : semi-conducteur « N » comme dans « doNNeur » ! Nous pouvons donc représenter schématiquement notre semi-conducteur N de la façon suivante :
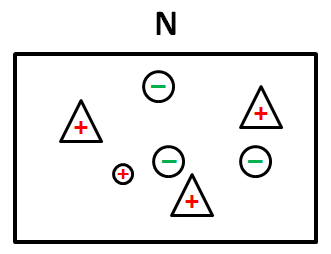
- les triangles « + » représentent les ions arsenic, c.-à-d. les atomes d'arsenic ayant perdu un électron,
- les grands ronds « − » représentent les porteurs majoritaires (électrons),
- les petits ronds « + » représentent les porteurs minoritaires (trous).
Les atomes de silicium ne sont pas représentés. Tout ce qui a été dit pour l'arsenic vaut également pour le phosphore, l'antimoine ou le bismuth qui possèdent eux aussi cinq électrons sur la couche externe de leurs atomes.
Et bien entendu, le cristal de silicium peut être remplacé par un cristal de germanium. << Causerie précédente Causerie suivante >> << Retour à la table des matières